MKN1细胞(人胃腺鳞癌细胞系MKN1)
MKN1细胞是由日本研究者Hojo,H.等人于1977年从一位72岁日本男性患者的胃部原发性腺鳞癌组织中分离建立的一种细胞系。该细胞系是研究胃癌,特别是腺鳞癌这一特殊亚型的生物学特性和治疗策略的重要体外模型。
细胞基本信息:
• JCRB编号:JCRB0252
• 组织来源:人胃(原发性)腺鳞癌
• 供体信息:72岁,日本男性
• 建立者:Hojo, H.
• 寄存者:Motoyama & Watanabe
• 寄存时间:1989年(寄存至JCRB年份)
• 特别说明:该细胞为经MC-210处理去除支原体的版本
细胞形态及生长特性:
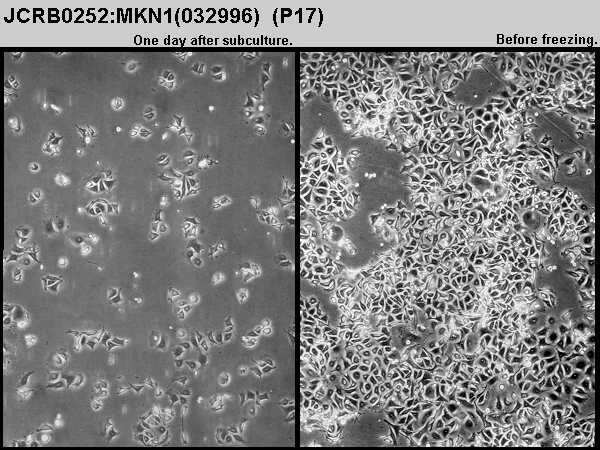
• 细胞形态:上皮样细胞
• 生长方式:贴壁生长
• 倍增时间:约30-36小时(不同批次略有差异,如LOT 03302009约30小时,LOT 01312012约35小时)
• 传代比例:建议1:10稀释传代(例如将一瓶80-90%融合的T-25培养瓶细胞传代至10瓶)
病毒污染检测:
通过实时荧光定量PCR检测病毒基因组片段,结果显示常见病毒(包括CMV、EBV、HBV、HCV、HIV-1/2、HTLV-1/2、HPV18、BKV、JCV、ADV、HAV、parvoB19等)均为阴性。
培养基:
• 基础培养基:90% RPMI-1640培养基
• 血清:10% 热灭活胎牛血清(FBS)
• 培养条件:37°C,5% CO₂
细胞培养注意事项:
1. 细胞复苏与接种密度
解冻复苏时,建议将整管细胞(约含1-3×10⁶个细胞)接种于T-25培养瓶或6cm培养皿中,使用推荐培养基。初始接种密度建议在2 - 6.5 × 10⁴ cells/mL范围内(参考LOT信息),以确保细胞能顺利进入对数生长期。
2. 传代操作
• 消化:细胞生长至80-90%融合时进行传代。吸弃旧培养基,用PBS(-)清洗一次后,加入0.25%胰蛋白酶 - 0.02% EDTA溶液,在37°C下消化约5-10分钟。
• 终止与接种:待细胞变圆、部分脱落时,立即加入含血清的新鲜培养基终止消化,轻轻吹打制成单细胞悬液。按1:10的比例稀释后接种至新培养瓶。
3. 换液频率
常规培养时,根据细胞生长速度和培养基颜色变化(酚红指示剂),通常每2-3天更换一次新鲜培养基。
4. 冻存方法
• 冻存液:BAMBANKER (LYMPHOTEC Inc., CS-02-001, NIPPON Genetics Co., LTD)。
• 冻存密度:推荐高密度冻存,建议每个冻存管内的细胞数不低于1×10⁶ cells/mL。
• 冻存步骤:使用程序降温盒(或逐步降温法:4°C 30分钟 → -20°C 1小时 → -80°C过夜)后,转移至液氮中长期保存。
5. 支原体污染
该细胞系在JCRB保存过程中已进行过支原体去除和检测,确保供应时无支原体污染。但培养过程中仍需严格遵守无菌操作规范,并建议定期自行检测。
细胞特性:
• 肿瘤类型:来源于胃部的腺鳞癌。腺鳞癌是一种同时具有腺癌和鳞状细胞癌成分的罕见胃癌类型,因此MKN1细胞是研究这种混合型肿瘤发生机制的宝贵模型。
• 基因特征:据相关文献(如 PMID: 3095279),该细胞系可用于检测胃癌细胞中扩增的DNA序列,提示其可能携带某些基因扩增,适合进行基因组不稳定性和癌基因研究。
• 同工酶分析:经JCRB检测,多种同工酶谱(如NP、G6PD、LD、AST、MD等)确认为人源,且G6PD为B型,排除了常见细胞交叉污染。
________________________________________
官方授权,渠道可查
自2006年起,比欧联科便与JCRB展开了合作。比欧联科凭借自身在国际运输、特殊物品和生物材料进口方面的专业优势,为用户提供外贸、物流、清关一体化解决方案,全方位保障细胞产品安全、准时送达用户手中。
JCRB现已正式授权比欧联科作为其在中国大陆地区的官方经销商,全面负责JCRB产品在中国的市场推广与销售工作。
极简流程,迅速到货
1. 客户确认需求
2. 与比欧联科签署进口协议
3. 比欧联科代办前置审批文件
4. 下单给JCRB
5. JCRB发货,比欧联科清关
6. 货物送达用户手中
________________________________________
参考文献
1. Hojo H, Oboshi S. Establishment of cultured cell lines of human stomach cancer origin and their morphological characteristics. Niigata Igkkai Zasshi, 91: 737-752, 1977.
2. Nakatani H, Tahara E, Yoshida T, et al. Detection of amplified DNA sequences in gastric cancers by a DNA renaturation method in gel. Jpn J Cancer Res. 1986 Sep;77(9):849-53. (PMID: 3095279)